Technological knowledge科技新知

超氧化物歧化酶(SuperOxide Dismutases, SODs)奧妙之處在於具有奪取及給予自由基電子的能力,也就是俗稱的歧化反應,能有效地清除生物體內的自由基。
而藍綠藻-最初進行光合作用的生物!!
24億年前為地球帶來大氧化事件,將大氣中不到1%的O2,轉化成如今約20%的比例,開啟生物演化重要的序章。生物在進行呼吸作用時,會有部分氧氣(O2)轉化成活性氧物質(Reactive Oxygen Species, ROS),進而產出各式各樣的自由基,藍綠藻為了抵抗自由基的傷害,演化出超氧歧化酶(SODs)以對抗自由基的傷害。
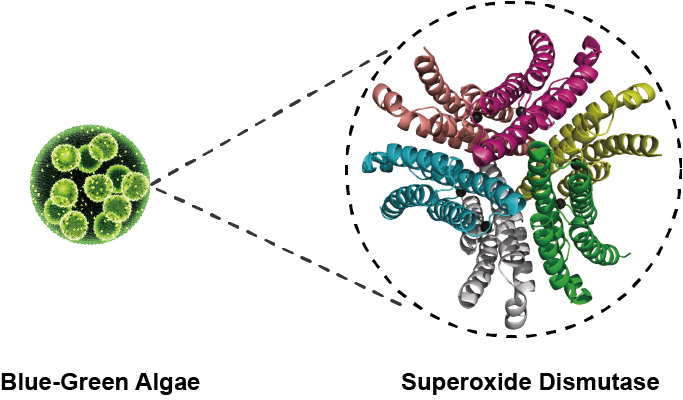
Fig.1 藍綠藻中SOD的蛋白質結構
1969年,Fridovich和McCord發現超氧化物歧化酶廣泛地存在於各類動物、植物、微生物中,可使細胞免於活性氧物質(ROS)攻擊而造成毀損或突變,在生物體中是極為重要的抗氧化劑。
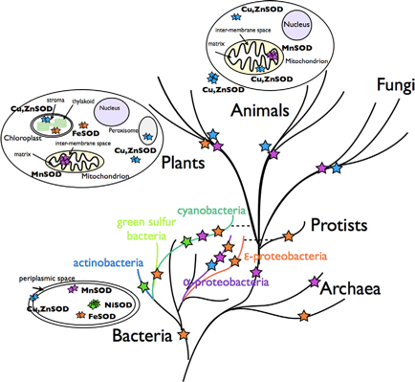
Fig.2 SOD物種分佈圖(FEBS Letters 2012, 586,585–595)
當超氧離子在生物體中濃度度升高時,超氧化物歧化酶將對其進行行歧化反應,並使其轉變為O2和H2O2(pH = 7 時,反應速度約為105 M−1s−1)。
SOD催化超氧化物的歧化反應可分為兩個步驟:
- 氧化反應:M(n+1)-SOD + O2− → Mn+-SOD + O2
- 還原反應:Mn+-SOD + O2− + 2H+ → M(n+1)-SOD + H2O2
其中M可為Cu(n=1)、 Mn(n=2)、 Fe(n=2)、Ni(n=2)等金屬離子,即超氧化物歧化酶具有銅/鋅、錳、鐵或鎳等四種活性中心。而在反應中,金屬的氧化態在n和n+1之間進行氧化反應與還原反應,達到有效清除活性氧物質的目的。
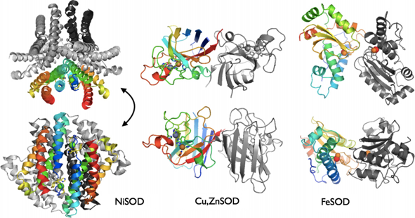
Fig.3 三種不同種類的SOD蛋白質結構(FEBS Letters 2012, 586,585–595)